第二章分子结构与性质第二节分子的立体构型.doc 55.00 KB
第二章分子结构与性质第二节分子的立体构型.ppt 325.50 KB
第二章分子结构与性质第二节分子的立体构型配合物.doc 42.00 KB
第二章分子结构与性质第二节分子的立体构型配合物.ppt 269.50 KB
第二章分子结构与性质第二节分子的立体构型杂化.doc 104.00 KB
第二章分子结构与性质第二节分子的立体构型杂化.ppt 1.21 MB
共3个课件,3份学案。
第二节分子的立体构型(第一课时学案)
[复习] 写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;
一、形形色色的分子
展示CO2、H2O、NH3、CH2O 、CH4分子的球棍模型(或比例模型);
二、价层电子对互斥理论()(Valence Shell Electron Pair Repulsion )
1、理论内容
(1)共价分子或离子的立体构型主要取决于。
(2)价层电子对包括
(3)价层电子对各自占据的位置倾向于彼此分离得尽可能的,此时电子对之间的斥力,整个分子最。
2、VSEPR的应用——预测分子或离子的立体构型
⑴确定中心原子价层电子对数目
价层电子对数=+
σ键电子对数=
孤电子对数=
a:
x:
b:
注意(1) 离子孤电子对数=
第二节分子的立体构型(第三课时学案)
复习:1、什么是配位键?
2、分析P41 实验
3、分析阳离子中成键情况
实验2-2
向CuSO4溶液中加入逐滴滴加氨水
离子方程式:
四、配合物理论简介
1、定义:
2、结构:
3、形成条件
⑴、
中心原子:可以是通常是
等
第二节分子的立体构型(第二课时学案)
复习:
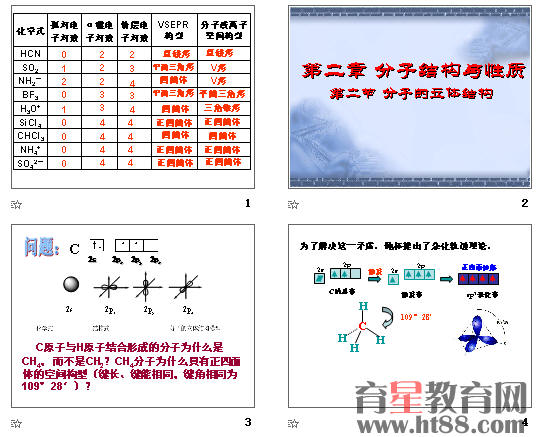
化学式
孤对电子对数 σ键电子对数 价层电子对数 VSEPR构型
(价层电子对构型) 分子或离子空间构型
HCN
SO2
NH2-
BF3
H3O+
SiCl4
CHCl3
NH4+
SO42-
三、杂化轨道理论
1、杂化轨道和杂化轨道理论的内容
⑴同一原子中的原子轨道在成键过程中重新组合,形成一系列
的新轨道的过程叫杂化。形成的新轨道叫
⑵能量相近通常指
⑶杂化轨道的数目等于
⑷原子轨道的杂化的过程中才会发生
⑸杂化轨道用于或
(6) 杂化轨道成键时要满足最大原理,最小原理
2、杂化的类型
⑴sp3杂化
①轨道和轨道杂化形成杂化轨道
②构型:
③实例:
⑵sp2杂化
①轨道和轨道杂化形成杂化轨道
②构型:
③sp2杂化的中心原子必有个垂直于σ骨架的,
该p轨道用于
④实例:
⑶sp杂化
①轨道和轨道杂化形成杂化轨道
②构型:





资源评论
共有 0位用户发表了评论 查看完整内容我要评价此资源