铁、铜及其化合物的应用(教案).doc
铁、铜及其化合物的应用.ppt
课件共11张,教案约2870字。
铁、铜及其化合物的应用(1)
【教学目标】
1、掌握铁、铜及其重要化合物的主要性质及应用。
2、通过思考与交流,实验和观察,科学探究、实践活动等,初步学会发现问题、提出问题、分析问题、解决问题,逐步培养敢于质疑、勇于创新的精神和合作精神等;
3、通过实验现象的推理分析,培养学生一切从实际出发,由表及里,以严密的逻辑推理得出结论的思维方法。
4、培养通过实验来研究物质及其变化的科学方法和严谨求实的科学态度;
【教学重点】
铁、铜的化学性质
【教学难点】
铁、铜的化学性质
【教学过程】
[引入]上节课我们我们了铁、铜的冶炼,那么铁、铜的性质又是怎样的呢?今天我们就来学习铁、铜的性质。
[板书]一、铁、铜的物理性质
[展示]铁片、铜片。
[观察]颜色、状态。
[讲述]纯铁是银白色的具有金属光泽的固体,密度较大,熔点较高;铜呈光亮的紫红色,具有金属光泽,密度较大,熔点较高。
[设问]铁、铜作为金属,还具有怎样的物理性质呢?
[讲解]具有金属的通性,如:能导电、导热,具有一定的延展性等等。
[板书]
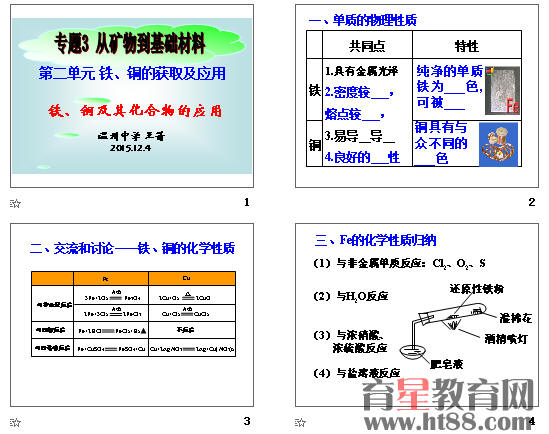
共同点 不同点
铁 具有金属光泽,密度较大,熔点较高,易导电、导热。 纯铁为银白色,有良好的延展性,质地较软,可被磁化
铜 铜具有与众不同的紫红色,质地较硬
[交流与讨论]在以前的学习中,我们已经了解了铁、铜与其它其它发生的一些反应,请你写出下列反应的化学方程式或离子方程式。你还知道有铁或铜参加的其它反应吗?将你所知道的反应填写在(5)、(6)的横线上。上述反应中,如果是氧化还原反应,请指出反应中的氧化剂和还原剂。
[提问]由上述反应分析:
(1)铁的活泼性如何?可用什么做判断依据?
(2)你曾经还学过铁的哪些化学性质?
[归纳]
(1)分析得出:用金属活动性顺序进行判断。与Na、Mg、Al、Cu比较得出结论。
(2)与Cl2、O2、盐酸(稀硫酸)、CuSO4溶液反应。
[板书]二、铁、铜的化学性质
1、铁的化学性质:铁是较活泼的金属(或中等活泼金属),在反应中充当还原剂。
[讲述]铁与氧化性较弱的氧化剂反应转化为+2价铁的化合物,而在与氧化性较强的氧化剂反应则转化为+3价铁的化合物。





资源评论
共有 0位用户发表了评论 查看完整内容我要评价此资源